Organik Kelompok:
Aldehida, keton, alkohol primer, dll
Kimia organik didominasi oleh " pendekatan kelompok fungsional ", di mana molekul organik dianggap akan dibangun dari:
- Sebuah kerangka hidrokarbon lembam ke mana kelompok fungsional (KT) yang terpasang atau ditumpangkan.
Pendekatan kelompok fungsional " bekerja" karena sifat dan kimia reaksi dari kelompok fungsional tertentu (FG) dapat sangat independen dari lingkungan.
Oleh karena itu, hanya diperlukan untuk mengetahui tentang kimia dari fungsi generik beberapa untuk memprediksi sifat kimia dari ribuan bahan kimia organik yang nyata.
Molekul organik juga bernama menggunakan pendekatan kelompok fungsional:
2-hexanone
2-heksanol
2-chlorohexane
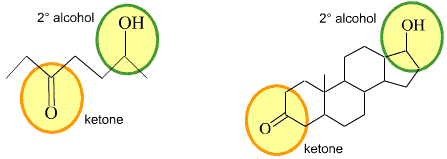
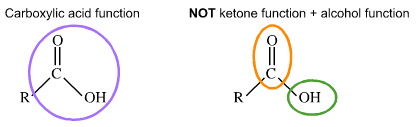
Aturannya adalah bahwa fungsi mengasumsikan identitas yang berbeda mereka ketika dipisahkan oleh -CH 2 - kelompok. Dengan demikian, karbonil, C = O, dan hidroksi, OH, asam karboksilat, RCOOH, merupakan bagian dari fungsi tunggal dan TIDAK "alkohol-plus-keton":
Sebuah Beberapa kata Tentang Fungsional Pendekatan Grup
Pendekatan kelompok fungsional adalah 100% empiris dalam hal itu ditentukan oleh eksperimen dan pengalaman, dan bukan oleh teori (seperti VSEPR, misalnya.)
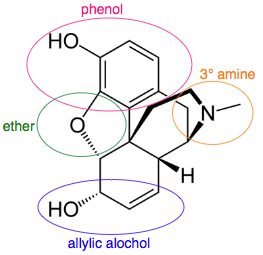
Sebuah entitas multifungsi seperti molekul obat morfin memiliki beberapa kelompok fungsional dan pusat kiral:
ahli kimia profesional pertimbangkan molekul organik multifungsi besar dalam hal 'substruktur' daripada kelompok fungsional.sistem cincin, misalnya, lebih baik dianggap sebagai substruktur, meskipun garis pemisah bisa kabur ...
Apa yang perlu Anda ketahui
Untuk menjadi mahir dalam kimia organik di tingkat masuk universitas [yaitu, Amerika AP, British A-Level atau Perancis Baccalaureate] sistem ujian,
dengan kata lain dapat:
nama molekul organik
memprediksi kelarutan dalam berbagai jenis pelarut
memprediksi reaktivitas kimia
memprediksi spektrum
Itu benar-benar penting untuk dapat mengenali 30 atau lebih fungsi yang tercantum di bawah. Untuk daftar yang lebih komprehensif KT organik, mencoba Chemogenesis Web Kitab FG database :
| Alkana |
Alkil, dan kadang-kadang aril (aromatik) fungsi diwakili oleh R yang
Metil: CH3? Ethyl: CH3CH2 Propyl:? CH3CH2CH2 Isopropyl: (CH3) 2CH? Phenyl: C6H5 dll
|
| Alkil halida |
Alkil halida [haloalkana] terdiri dari gugus alkil yang melekat pada halogen:
F, Cl, Br, I. Kloro, bromo dan iodo alkil halida sering mengalami eliminasi dan / atau reaksi substitusi nukleofilik.
|
| Alkohol primer |
Alkohol primer memiliki fungsi -OH terikat pada kelompok R-CH2-.
Alkohol primer dapat dioksidasi menjadi aldehid dan asam karboksilat. (Ini bisa sulit untuk menghentikan oksidasi pada tahap aldehida.) Alkohol primer dapat ditampilkan dalam teks sebagai: RCH2OH |
| Alkohol sekunder |
Alkohol sekunder memiliki fungsi -OH terikat pada kelompok R2CH-.
Alkohol sekunder dapat dioksidasi menjadi keton. Alkohol sekunder dapat ditampilkan dalam teks sebagai: R2CHOH |
| Alkohol tersier |
Alkohol tersier memiliki fungsi -OH terikat pada kelompok R3C-.
Alkohol tersier tahan terhadap oksidasi dengan diasamkan kalium dikromat (VI), K. Alkohol tersier dapat ditampilkan dalam teks sebagai: R3COH |
| Aldehida |
Aldehida memiliki hidrogen dan alkil (atau aromatik) kelompok yang melekat pada fungsi karbonil.
Aldehida dapat ditampilkan dalam teks sebagai: RCHO Aldehid mudah teroksidasi menjadi asam karboksilat, dan mereka dapat dikurangi menjadi alkohol primer. Aldehida dapat dibedakan dari keton dengan memberikan hasil tes positif dengan solusi Fehlings (bata merah endapan) atau Tollens reagen (cermin perak). Aldehida memberikan merah-oranye endapan dengan 2,4-dinitrophenyl hidrazin. |
| Keton |
Keton memiliki sepasang gugus alkil atau aromatik melekat fungsi karbonil.
Keton dapat ditampilkan dalam teks sebagai: RCOR Keton dapat dibedakan dari aldehida dengan memberikan hasil tes negatif dengan Fehling? S solusi (bata merah endapan) atau Tollens reagen (cermin perak). Keton memberikan merah-oranye endapan dengan 2,4-dinitrophenyl hidrazin.
|
| Asam karboksilat |
Asam karboksilat memiliki alkil atau kelompok aromatik melekat fungsi hidroksi-karbonil.
Asam karboksilat dapat ditampilkan dalam teks sebagai: RCOOH Asam karboksilat adalah asam Bronsted lemah dan mereka membebaskan CO2 dari karbonat dan karbonat hidrogen.
|
| Fungsi karbonil |
Gugus karbonil adalah fungsi yang super karena banyak kelompok fungsional umum didasarkan pada karbonil, termasuk:
Aldehida, keton, asam karboksilat, ester, amida, asil (asam) klorida, asam anhidrida
|
| Ester |
Ester memiliki sepasang alkil atau kelompok aromatik yang melekat pada fungsi oksigen karbonil + menghubungkan.
Ester dapat ditampilkan dalam teks sebagai: RCOOR atau (kadang-kadang) ROCOR. asam karboksilat + alkohol -> ester + air Ini adalah asam katalis kesetimbangan.
|
| Amida |
Amida primer (ditampilkan) memiliki alkil atau gugus aromatik melekat fungsi amino-karbonil.
Amida primer dapat ditampilkan dalam teks sebagai: RCONH2 Amida sekunder memiliki alkil atau aril yang terikat pada nitrogen: RCONHR Amida tersier telah dua alkil atau aril yang terikat pada nitrogen: RCONR2
|
| Amina primer |
Amina primer memiliki alkil atau gugus aromatik dan dua atom hidrogen yang terikat pada atom nitrogen.
Amina primer dapat ditampilkan dalam teks sebagai: RNH2 Amina primer adalah fungsi dasar yang dapat terprotonasi dengan ion amonium yang sesuai. Amina primer juga nukleofilik.
|
| Amina sekunder |
Amina sekunder memiliki sepasang alkil atau kelompok aromatik, dan hidrogen, yang melekat pada atom nitrogen.
Amina sekunder dapat ditampilkan dalam teks sebagai: R2NH Amina sekunder adalah fungsi dasar yang dapat terprotonasi dengan ion amonium yang sesuai. amina sekunder juga nukleofilik.
|
| Amina tersier |
Amina tersier memiliki tiga gugus alkil atau aromatik yang melekat pada atom nitrogen.
Amina tersier dapat ditampilkan dalam teks sebagai: R3N Amina tersier adalah fungsi dasar yang dapat terprotonasi dengan ion amonium yang sesuai. Amina tersier juga nukleofilik.
|
| Asam klorida |
Asam klorida, atau asil klorida, memiliki alkil (atau aromatik) kelompok yang melekat pada fungsi karbonil ditambah labil (mudah dipindahkan) klorin.
Asam klorida yang sangat entitas reaktif sangat rentan terhadap serangan nukleofil. Asam klorida dapat ditampilkan dalam teks sebagai: R-COCl atau RCOCl |
| Asam anhidrida |
Anhidrida asam terbentuk ketika air akan dihapus dari asam karboksilat, maka nama itu.
Anhidrida asam dapat ditampilkan dalam teks sebagai: (RCO) 2O
|
| Nitrile |
Nitril (atau sianida organo) memiliki alkil (atau aromatik) kelompok yang melekat pada fungsi karbon-triple-ikatan-nitrogen.
Nitril dapat ditampilkan dalam teks sebagai: RCN Perhatikan bahwa ada masalah nomenklatur dengan nitril / sianida. Jika senyawa disebut sebagai nitrile maka karbon nitrile dihitung dan dimasukkan, tetapi ketika senyawa ini disebut sebagai sianida tidak. Sebagai contoh: CH3CH2CN disebut propana nitrile atau etil sianida (cyanoethane). |
| Ion karboksilat atau garam |
Ion karboksilat adalah basa konjugat dari asam karboksilat, yaitu. asam karboksilat yang terdeprotonasinya.
Ion karboksilat dapat ditampilkan dalam teks sebagai: RCOO? Ketika ion kontra disertakan, garam sedang ditampilkan. Garam dapat ditampilkan dalam teks sebagai: RCOONa |
| Ion amonium |
Ion amonium memiliki total empat alkil dan / atau hidrogen fungsi yang melekat pada atom nitrogen.
[NH4] + [RNH3] + [R2NH2] + [R3NH] + [R4N] + ion amonium kuaterner tidak donor proton, tapi yang lain adalah asam Bronsted lemah (pKa sekitar 10). |
| Asam amino |
Asam amino, ketat asam alpha-amino, memiliki asam karboksilat, fungsi amino dan hidrogen yang terikat pada atom karbon yang sama.
Ada 20 alami asam amino. Semua kecuali glisin (R = H) adalah kiral dan hanya L enantiomer ditemukan di alam. Asam amino dapat ditampilkan dalam teks sebagai: R-CH (NH2) COOH
|
| Alkena |
Alkena terdiri dari fungsi ikatan rangkap C = C.
Alkena dapat ditampilkan dalam teks sebagai: Mono diganti: RCH = CH2 1,1-tersubstitusi: R2C = CH2 1,2-tersubstitusi: RCH = CHR Alkena adalah planar dan tidak ada rotasi ikatan C = C. Alkena adalah elektron pusat reaktif kaya dan rentan terhadap penambahan elektrofilik. |
| Trans-Alkene |
Trans-alkena adalah fungsi 1,2-Disubstituted dengan dua R, X atau kelompok lain di sisi berlawanan dari C fungsi = C.
Karena non-rotasi ikatan C = C, cis dan isomer geometrik trans tidak [termal] Interconverted. |
| Cis-Alkene |
Cis-Alkena adalah fungsi 1,2-Disubstituted dengan dua R, X atau kelompok lain pada sisi yang sama dari C fungsi = C.
Karena non-rotasi ikatan C = C, cis dan isomer geometrik trans tidak [termal] Interconvertion. |
| Eter |
Eter memiliki sepasang gugus alkil atau aromatik yang melekat pada atom oksigen menghubungkan.
Eter dapat ditampilkan dalam teks sebagai: ROR Eter secara mengejutkan tidak aktif dan sangat berguna sebagai pelarut untuk banyak banyak (tetapi tidak semua) kelas reaksi. |
| Ion alkoksida |
Alkoksida ion gugus alkil melekat pada oxyanion.
ion alkoksida dapat ditampilkan dalam teks sebagai: RO? Alkoksida natrium, Rona, adalah basis sedikit lebih kuat dari air sehingga tidak dapat disiapkan dalam air.Sebaliknya mereka siap dengan menambahkan natrium ke alkohol kering. |
| Hidroksinitril |
Hydroxynitriles (juga disebut cyanohydrins) terbentuk ketika hidrogen sianida, H + CN ?, menambahkan seluruh fungsi karbonil aldehida atau keton. |
| Karbokation primer |
Karbokation primer memiliki fungsi alkil tunggal melekat ke pusat karbon dengan muatan positif formal.
Karbokation - juga dan lebih tepat disebut ion karbenium - yang intermediet reaktif penting yang terlibat dalam reaksi adisi elektrofilik dan reaksi substitusi aromatik elektrofilik. Stabilitas: primer << sekunder << tersier |
| Karbokation sekunder |
Karbokation sekunder memiliki sepasang fungsi alkil melekat ke pusat karbon dengan muatan positif formal.
Karbokation - juga dan lebih tepat disebut ion karbenium - yang intermediet reaktif penting yang terlibat dalam reaksi adisi elektrofilik dan reaksi substitusi aromatik elektrofilik. Stabilitas: primer << sekunder << tersier |
| Karbokation tersier |
Karbokation tersier memiliki tiga fungsi alkil yang terikat pada pusat karbon dengan muatan positif formal.
Karbokation - juga dan lebih tepat disebut ion karbenium - yang intermediet reaktif penting yang terlibat dalam reaksi adisi elektrofilik dan reaksi substitusi aromatik elektrofilik. Stabilitas: primer << sekunder << tersier |
| Asil kation |
Kation asil memiliki alkil (atau aromatik) kelompok yang melekat pada fungsi karbonil dengan muatan positif formal.
Kation asil yang intermediet reaktif penting dan terlibat dalam reaksi adisi elektrofilik dan reaksi substitusi aromatik elektrofilik. Kation asil biasanya terbentuk dari asil yang sesuai / asam klorida ditambah aluminium klorida. |
| Polimer |
Polimer terdiri dari molekul-molekul monomer kecil yang bereaksi bersama-sama sehingga membentuk struktur kovalen besar.
Ada dua jenis umum dari polimerisasi: penambahan dan kondensasi. polimer rantai linier umumnya termoplastik, sementara tiga polimer jaringan dimensi tidak. |
| Diol atau poliol |
Diol dan poliol adalah alkohol dengan dua atau lebih fungsi -OH.
Diol dan poliol sangat larut dalam air. Mereka digunakan sebagai suhu tinggi pelarut polar. |
Source: http://www.chemistry-drills.com/functional-groups.php